Цикл тепловой машины, рабочим веществом которой является 




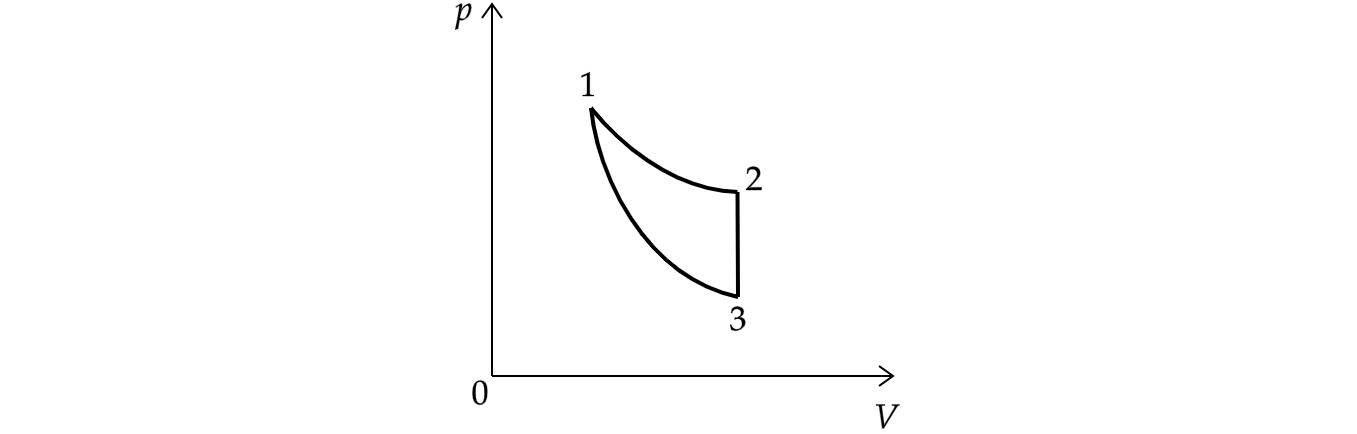
Процессы:
1-2 — изотермический
2-3 — изохорный
3-1 — адиабатический
КПД тепловой машины равен:

где 

Работа газа за цикл есть сумма работ газа в каждом процессе:

Так как в процессе 2-3 объем газа постоянен, то его работа равна нулю.
Тогда работа газа за цикл равна:

Далее необходимо найти количество теплоты 
Для этого запишем первое начало термодинамики для каждого процесса.
Процесс 1-2:

Так как процесс 1-2 изотермический, то изменение внутренней энергии газа 
Объем газа увеличивается, следовательно, газ совершает положительную работу.
Отсюда получаем, что:

Так как процесс 2-3 изохорный, то работа газа 
Давление газа уменьшается, следовательно, его температура также уменьшается (для изохорного процесса 
Следовательно, изменение внутренней энергии газа отрицательно.
Отсюда получаем, что:

Процесс 3-1:
Так как процесс 3-1 адиабатный, то 

Таким образом, количество теплоты, полученное газом от нагревателя равно:


Подставим (2), (4) в (1):


Подставим (3) в (5):

Изменение внутренней энергии газа в процессе 3-1 равно:

где 
Подставим (7) в (6) и выразим искомую температуру:


Температура 

Следовательно, температура 

Работа 

Таким образом, искомая температура равна:

