На диаграмме 
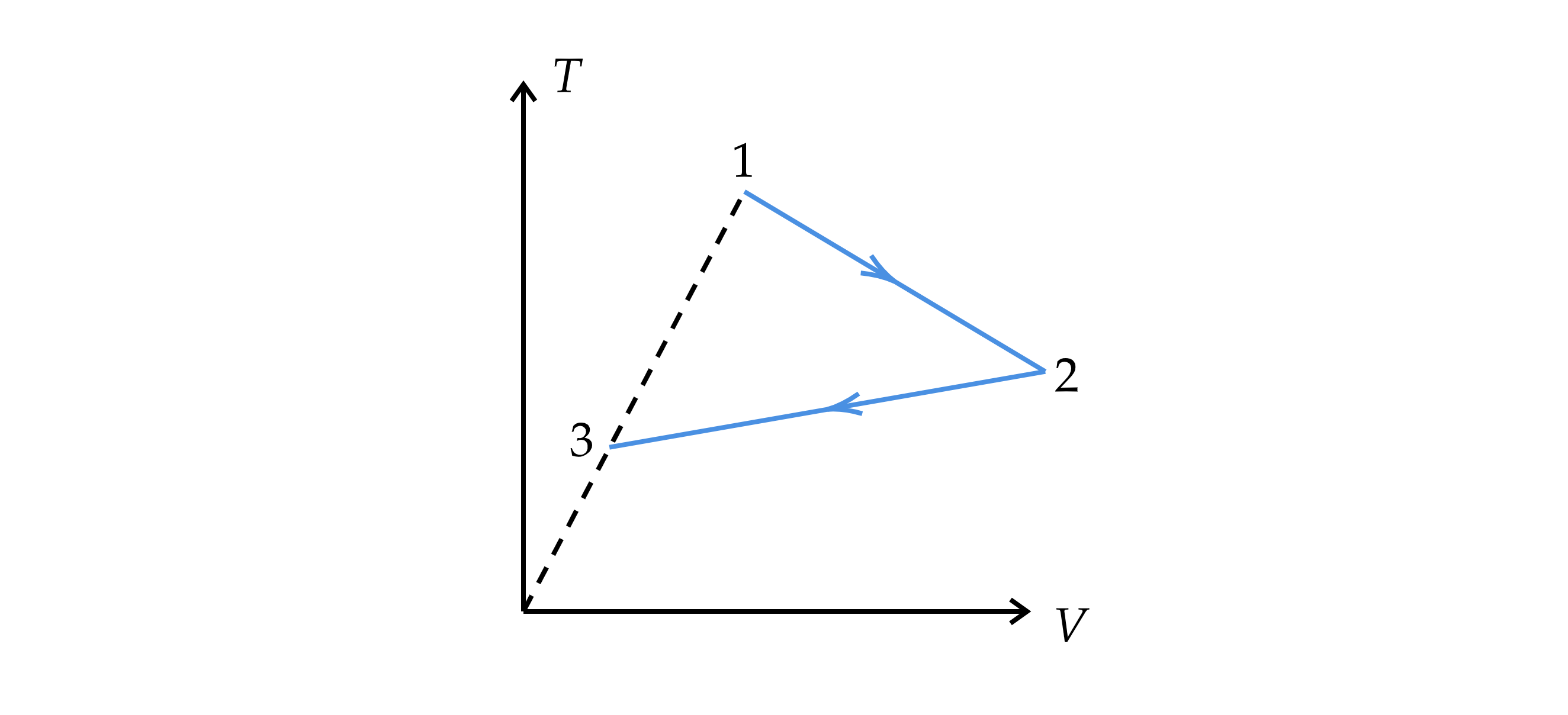
Проведем две прямые через начало координат так, как показано на рисунке
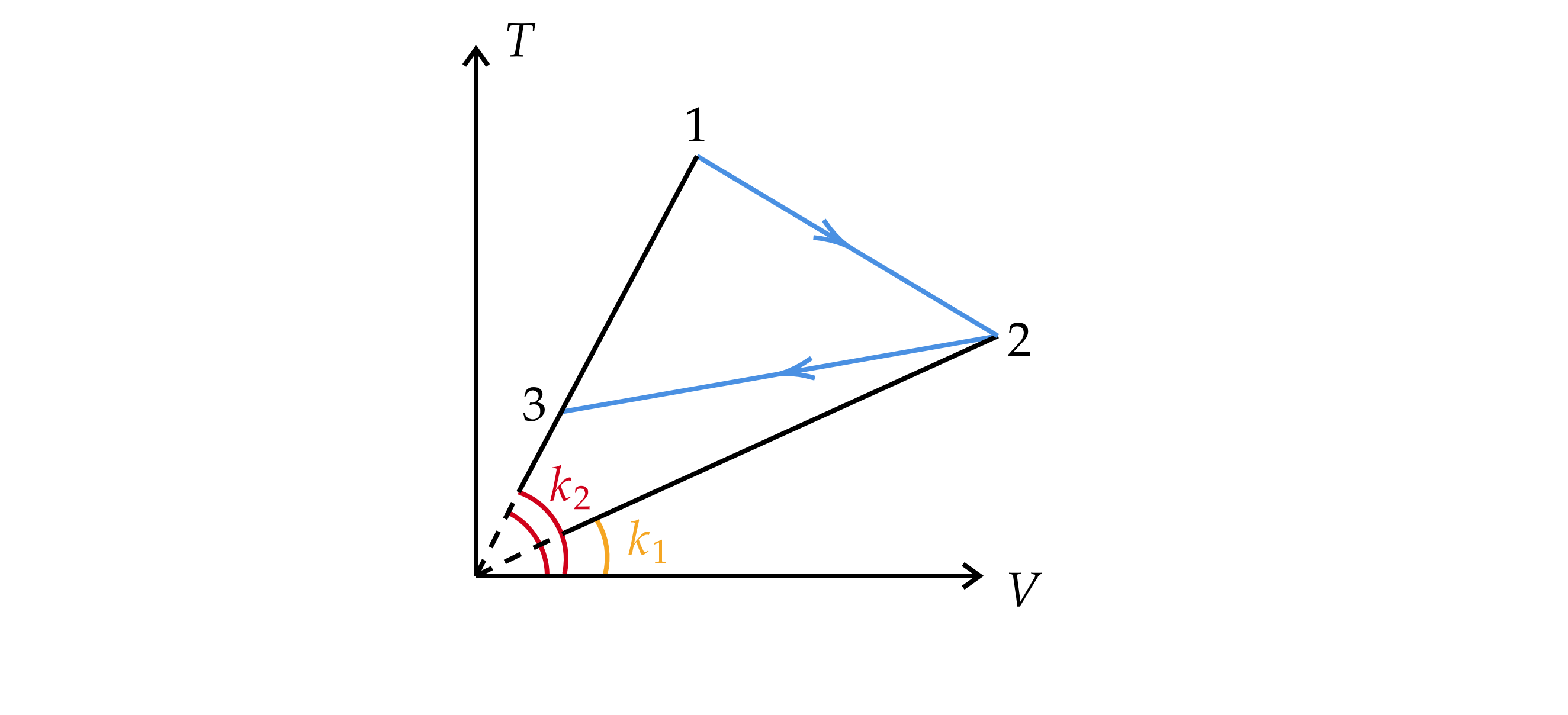
Запишем уравнение Менделеева-Клапейрона:

где 



Давление из уравнения Менделеева-Клапейрона равно:

При этом прямые описываются уравнением:

Тогда

то есть давление в точках 1 – 3 описывает только с помощью угловых коэффициентов. Так как точки 1 и 3 лежат на одной прямой, то давление в них одинаково, при этом 
